你一定經常聽說維生素的正論反論,是是非非(英文有個貼切的描述:minus-plus,也可以理解成褒貶不一),因為一些人覺得他們無所不能,而另一些人卻堅持認為B族維生素根本沒有用處。比如經常口腔潰瘍,是缺維生素B了吧,但吃青菜也挺多的呀/還經常吃復合維生素B,為什么會缺呢?
事實上,人體的B維生素主要是通過食物獲得(哪些食物維生素B含量最高?怎樣減少烹飪造成的B族維生素損失?),不管是蔬菜、水果、堅果、全谷類、豆類、蛋奶類、魚蝦類和瘦肉中都含有豐富的B族維生素,同時腸道微生物通過正常的營養進食也能幫忙合成大部分B族維生素。

那為什么還有人會缺B族維生素呢?對于人體獲得的維生素(不管是天然食物中,補充劑還是微生物合成的),其獲益者(或者說利用者)不只是人體自身,還有腸道里的微生物。最近的一項研究給我們帶來了啟示:在缺乏膳食纖維的飲食情況下,你腸道中的微生物會跟你爭奪B族維生素,讓你自體利用能力下降甚至全部被剝奪。
文章:Dietary fibers boost gut microbiota-produced B vitamin pool and alter host immune landscape
雜志:Microbiome
日期:2024年9月23日
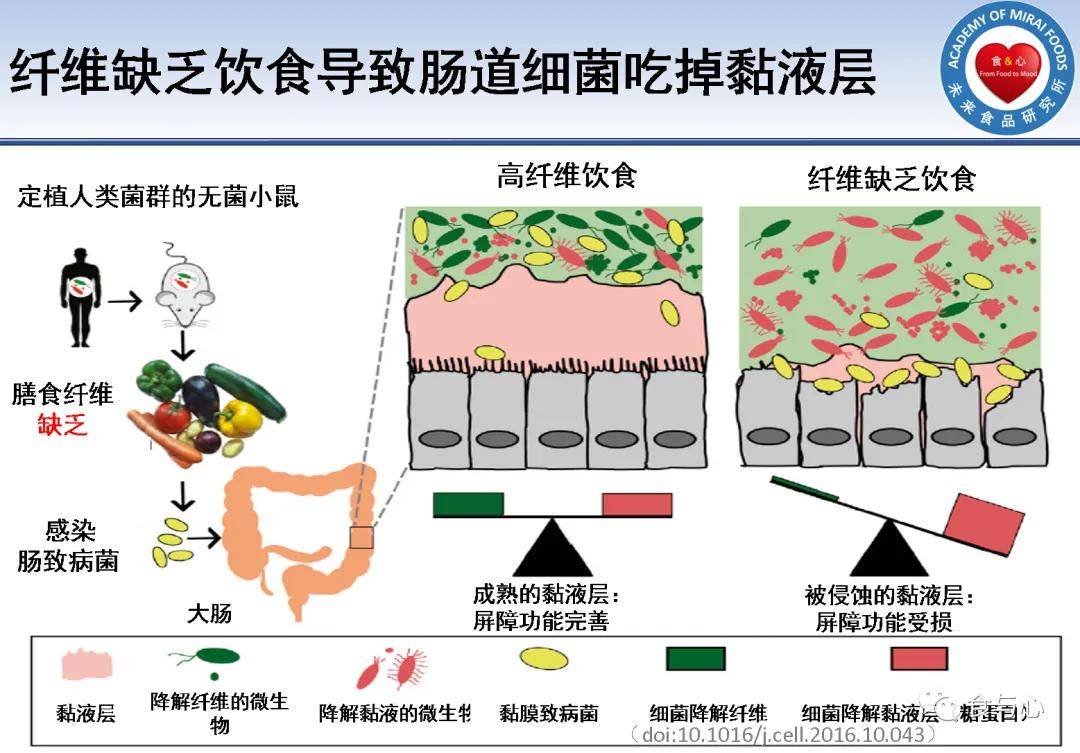
早就有研究發現,膳食纖維是微生物和免疫穩態的關鍵驅動因素。缺乏膳食纖維本身就會改變腸道細菌組成,導致腸道侵蝕黏液層的細菌增加,削弱腸道屏障功能,降低抗感染能力(飲食缺乏膳食纖維不僅僅會引起便秘,還會降低抗感染能力)。
B族維生素參與許多宿主生化和代謝途徑,具有重要的免疫調節特性 。硫胺素(維生素 B1)是三羧酸 (TCA) 循環中的關鍵輔助因子,幼稚免疫細胞和調節免疫細胞優先使用硫胺素免疫細胞來獲取能量。核黃素(維生素 B2)具有全身性抗炎特性 ,主要是通過減少腸道中的氧氣,允許宿主有益纖維降解細菌的生長。煙酸酯(維生素 B3)與 SCFA 丁酸鹽一樣,通過 GPCR109a 發出信號,抑制促炎細胞因子的產生并在 cLP 中誘導 Treg 細胞(調節性T細胞)。泛酸(維生素B5)是輔酶A的前體,可促進CD8 Tc22極化,從而增強抗腫瘤免疫力和抗結核分枝桿菌感染能力。維生素 B6 包括吡哆醇、吡哆醛、吡哆胺及其磷酸化衍生物,在多種免疫疾病(包括關節炎和結腸癌)中表現出抗炎特性。維生素B6還能通過減少IL-1β的產生并進一步抑制 NLRP3 炎性小體的激活來保護小鼠免于內毒素休克。
研究者設計了一套精密的實驗,探索飲食和腸道微生物對于宿主可用的B族維生素的影響。
研究中使用了三種不同菌群定植狀態的小鼠,包括:
GF小鼠——無菌小鼠
SPF小鼠——無特定病原體小鼠,擁有正常菌群
14SM小鼠——只擁有少量和有限的腸道微生物的小鼠,包括阿克曼菌等14種細菌。
研究中使用了5種不同的飲食,區別主要在于有無膳食纖維及纖維類別:
FF飲食——無纖維飲食
IN飲食——用菊粉替代了FF中10%的葡萄糖的飲食
FS飲食——用粗纖維替代了FF中10%的葡萄糖的飲食,粗纖維是自于蘋果、小麥、燕麥、豌豆和洋車前子的等量粗纖維混合物。
SC飲食——標準飲食。SC1和SC2來自不同廠家,除了膳食纖維種類的差別,其他營養成分相同。研究發現:
腸道細菌定植狀態和飲食都對宿主免疫產生了明顯影響,包括腸道固有層、脾臟和肺的免疫細胞類群,當然對腸道的影響最大。另外菌群的影響還要強于飲食。
原本相同飲食的SPF小鼠,40天不同飲食后,標準飲食(SC飲食)的小鼠腸道中富集了降解纖維的菌,比如Prevotellaceae、Lachnospiraceae、Muribaculaceae 和 Eubacterium 。而無纖維飲食(FF飲食)的小鼠腸道中富集了降解黏液蛋白的菌,比如瘤胃球菌科和阿克曼菌。兩組小鼠的腸道免疫細胞類群不同,FF飲食小鼠的特征是肥大細胞、CD11c 細胞、總ILC、總T細胞、CD62LCD44 T細胞、LyC6CD8 T 細胞(CD44 +)和CD4 T細胞增加。
原本相同飲食的SPF小鼠,40天不同飲食后,腸道微生物發生了明顯區別,菊粉飲食(IN飲食)小鼠腸道富集了大量產生丁酸的細菌。與FF飲食小鼠相比,IN飲食和FS飲食(粗纖維飲食)小鼠腸道免疫細胞類群明顯不同,脾臟和肺的免疫細胞類群也不相同。比如脾臟中的Th(輔助性T細胞)和Treg亞群隨纖維類型而變化,其中Th17細胞、Tbet-Treg 和 RORgt+Treg 在菊粉飲食組中富集,而Th2細胞和 GATA3-Treg則在 SC2 和FS組中富集;與標準飲食SC1組相比,FF飲食組肺中總T細胞和各種亞群(即 CD44++-CD62L、CD5和CD8)水平升高。
與其他4種纖維飲食相比,無纖維飲食(FF飲食)小鼠的短鏈脂肪酸(SCFA)合成能力受損。與 SC1組相比,FF組的盲腸乙酸鹽、丁酸鹽和丙酸鹽明顯降低,而異丁酸酯和異戊酸酯(即支鏈氨基酸微生物代謝衍生的支鏈脂肪酸)顯著增加增加。且FF組小鼠盲腸中次級膽汁酸顯著減少。
5種飲食組相比,在微生物組和盲腸代謝組方面,菊粉飲食(IN飲食)與兩種標準化飲食組更為相似。IN飲食和兩種標準化飲食組的B族維生素明顯增加,而在FF和FS喂養的小鼠中,B族維生素的濃度降低或不存在。具體而言,SC1、SC2 和IN組核黃素(維生素 B2)、煙酸酯(維生素 B3 )、泛酸酯(維生素 B5)和維生素B6的濃度較高,而FS和FF組幾乎不存在。
宏代謝組學分析顯示,FF組小鼠盲腸B族維生素合成減少而消耗增加。與IN組相比,FF組葉酸和B12合成能力減小,而B2、B3、B7利用能力增加。與FF組相比,IN組B1、B2、B3、B7和B12的參與合成/利用比率更高; SC2組B2、B3、葉酸/B9和B12的合成/利用比率更高。在這三組中,負責合成和降解維生素的微生物種類明顯不同。
小結:腸道微生物不僅是腸道屏障的關鍵組分,還在局部和全身免疫、膽汁酸代謝以及維生素B的合成中發揮著重要作用。膳食纖維不僅是有益微生物的食物,還能增強宿主免疫,促進腸道微生物合成短鏈脂肪酸和次級膽汁酸,提升腸道微生物合成B族維生素的能力而降低微生物利用B族微生物的能力,從而增加宿主的B族微生物可獲得性。
由此不難理解那些又吃復合維生素B又大量吃蔬菜,但體檢依然發現缺維生素B的人,肚子里那些跟人爭搶B族維生素的細菌可能是關鍵。
食與心溫馨總結:腸道微生物能幫助宿主合成B族維生素,也能跟宿主爭搶B族維生素。為了自體B維生素的需求,我們不僅需要攝入維生素,還需要控制腸道那些掠奪維生素的菌,來保證人體的維生素供給,維持免疫、代謝、內分泌、神經、和皮膚等功能的健康。
抑制B族維生素搶奪者的方法其實很簡單,就是增加食物中的膳食纖維攝入。充足的膳食纖維攝入,不僅能調節腸道菌群,增強腸道屏障功能,提升免疫力,還能合成短鏈脂肪酸、次級膽汁酸和B族維生素。而缺乏膳食纖維,不僅會削弱腸道屏障功能,降低免疫力,還會在腸道培養出一群跟人搶奪B族微生物的細菌,從而減少人體可用的維生素量。
由于不同種類的膳食纖維對腸道微生物的影響不同,日常飲食中攝入多種不同的膳食纖維食物更能促進菌群多樣化,增強B族維生素合成能力。簡單理解就是,不要想著只有蔬菜水果中才含有維生素B,除了這兩類,菌菇類、豆類、全谷類和堅果等不僅也含有維生素B,其中的膳食纖維還能促進腸道菌群合成維生素B,從而進一步增加人體維生素B的可獲得性。

雖然肉類、奶蛋類、精米白面中也都含有B族維生素,人也能直接口服維生素B補劑,但這些食物中缺乏膳食纖維。如果長期吃精加工碳水(精米白面)、甜食和肉食,即便服用復合維生素B補劑也往往難以滿足身體的需求,因為這些維生素B會先被腸道細菌利用,剩下的才能被吸收供人體使用。
以上實驗也證明了缺少膳食纖維的飲食還能改變腸道微生物結構,養出來更多搶奪B族維生素的細菌。
經常有人跟食與心抱怨,自己的免疫力低下,口腔潰瘍此起彼伏,從不間歇。這種情況下應該首先反思自己的飲食出了什么問題。皮膚或者口腔出了問題時,單獨補充維生素往往難以取得理想效果,長期的飲食調整才能從根本上解決經常皮炎、口腔潰瘍等問題。

