轉(zhuǎn)自:北京青年報(bào)客戶端
內(nèi)臟器官疾病的精準(zhǔn)治療依賴于高效藥物遞送方法。北京航空航天大學(xué)生物與醫(yī)學(xué)工程學(xué)院常凌乾團(tuán)隊(duì)與合作者研發(fā)了一種柔性可植入式電子貼片(NanoFLUID),融合了柔性電子、微納加工等前沿技術(shù),具有無線控制、極致輕薄和易貼附特點(diǎn),可以像創(chuàng)可貼一樣貼在生物體器官上,將藥物精準(zhǔn)送達(dá)靶器官部位和細(xì)胞內(nèi)部。相關(guān)成果4月30日發(fā)表于頂級(jí)學(xué)術(shù)期刊《自然》(Nature)。
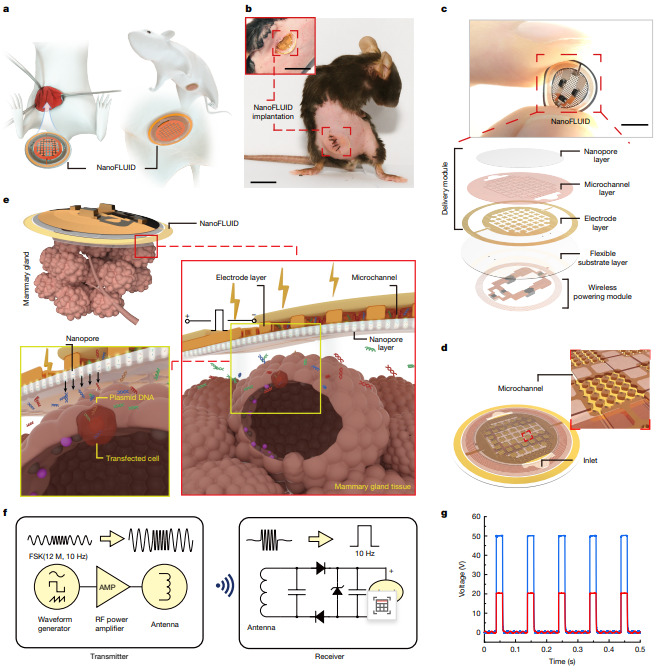
NanoFLUID實(shí)現(xiàn)內(nèi)臟器官精準(zhǔn)給藥
現(xiàn)有的藥物遞送范式面臨兩大挑戰(zhàn):傳統(tǒng)的口服或者靜脈給藥方式效率有限,藥物在全身循環(huán)中容易"迷路",難以精準(zhǔn)到達(dá)病灶部位,并產(chǎn)生對(duì)其它器官損傷的風(fēng)險(xiǎn);大分子藥物如基因藥物,很難穿過細(xì)胞膜天然屏障。“按照常規(guī)的給藥方式,相當(dāng)于吃100塊錢的藥,可能只有1塊錢的藥能真正到達(dá)病灶區(qū)域進(jìn)行有效治療。”北航生物與醫(yī)學(xué)工程學(xué)院常凌乾教授解釋道。

北航基于NanoFLUID的技術(shù)轉(zhuǎn)化:Ultra-NEP透皮導(dǎo)入儀
為解決這一問題,常凌乾團(tuán)隊(duì)聯(lián)合北京大學(xué)、香港城市大學(xué)、美國伊利諾伊大學(xué)厄巴納-香檳分校、西北工業(yè)大學(xué)等研究者研發(fā)的這種NanoFLUID,基于常凌乾團(tuán)隊(duì)標(biāo)簽技術(shù)——納米電穿孔,通過結(jié)合柔性電子材料,形成5層微納結(jié)構(gòu)電子貼片,中間層為藥倉,可直接附著在器官表面。其獨(dú)特的“納米孔-微通道-微電極”的3D結(jié)構(gòu),可實(shí)現(xiàn)低電壓下細(xì)胞膜安全穿孔,同時(shí)巧妙利用納米孔道內(nèi)形成的超高電場強(qiáng)度,將藥物分子遞送速度提升了上萬倍(對(duì)比傳統(tǒng)的電遞送方法)。無源供電模塊保證了貼片在植入內(nèi)臟器官后的實(shí)時(shí)可控打開細(xì)胞膜“通道”,將大分子或基因藥物分子以高于傳統(tǒng)遞送速度安全、快速高效送入目標(biāo)細(xì)胞內(nèi)。NanoFLUID還可以通過調(diào)控電參數(shù),精準(zhǔn)地以微米和微克為單位控制藥物進(jìn)入器官的深度及劑量。
NanoFLUID代表了一項(xiàng)具有范式革新意義的生物電子學(xué)突破,為內(nèi)臟器官靶向治療開辟了新途徑。該技術(shù)目前已在北航實(shí)現(xiàn)轉(zhuǎn)化,應(yīng)用在醫(yī)學(xué)美容、皮膚創(chuàng)傷修復(fù)等領(lǐng)域,孵化了基于納米電穿孔的無創(chuàng)Ultra-NEP透皮導(dǎo)入儀,實(shí)現(xiàn)高效藥物遞送。
常凌乾團(tuán)隊(duì)目前正在研究可降解材料,以便貼片在使用后可自行降解。團(tuán)隊(duì)還致力于提高貼片與復(fù)雜器官表面的貼合度,以及開發(fā)無創(chuàng)植入方式,如利用微型機(jī)器人(16.660, 0.49, 3.03%)或微導(dǎo)管對(duì)貼片進(jìn)行精準(zhǔn)導(dǎo)航到目標(biāo)位置。該項(xiàng)成果是典型的醫(yī)工交叉的成果,涉及到細(xì)胞生物學(xué)、基因工程、電子、力學(xué)、微納加工和材料學(xué)等學(xué)科,體現(xiàn)了北航的現(xiàn)代生物醫(yī)學(xué)工程學(xué)科群逐漸地向多學(xué)科有機(jī)融合的發(fā)展趨勢。
文/北京青年報(bào)記者 雷嘉


